Kvantinė fizika: Atomas
Na va. Po tiek straipsnių apie fundamentaliąsias daleles pakalbėsime apie \“milžinišką\“ atomą. Labai svarbu paminėti, kad kvantiniai procesai veikia tik itin mažais atstumais, maždaug 1-5 angstremų (10^-15 m). Čia susipažinsime su vienu iš jų . Tiesą sakant apie kvantinę mechaniką dar net nepradėjom kalbėti :).
Atomo modeliai
Na kaip jau minėjau pirmame straipsnyje žmonės graikų laikais įsivaizdavo atomą kaip mažą nesuskaldomą kamuoliuką. Po to buvo sukurtas labai keistas, vadinamas \“pudingo su razinom\“ modelis. Remiantis šiuo modeliu atomai buvo panašūs į amebas, su labai tankia, teigiamai įelektrinta medžiaga (panašiai kaip citoplazma) ir neigiamai įelektrintais mažais kamuoliukais \“prilipusiais\“ prie jos (elektronais). Šis modelis paaiškina branduolio stabilumą ir dalijimosi mechanizmą tačiau nėra tinkamas, nes branduolinis \“skystis\“ turėtų būti kvantinis (sudarytas iš kažkokių dalelių).

Tada mokslininkas Rezerfordas (Rutherford) pabandė rasti atomo analogiją kažkur visatoje ir paskelbė klasikinės saulės sistemos modelį. Šis modelis teigė, kad tarsi planetos dėl gravitacijos besisukančios aplink žvaigždę, elektronai sukasi aplink branduolį dėl elektromagnetinės saveikos. Šio modelio iškarto buvo atsisakyta, nes jis turėjo gan komišką problemą. Pagal šį modelį visi elektronai turėtų vos per keletą sekundžių nukristi į banduolį. Tokie atomai egzistuoti negalėtų.

Kitą, žymiai tobulesnį modelį pasiūlė mokslininkas Boras (Bohr). Jis pateikė postulatą, kad atomas yra suskirstytas energijos lygmenimis ir elektronas gali egzistuoti tik viename iš jų (kaip negalime giventi tarp daugiaaukščio namo aukštų). Kad elektronas patektų į aukštesnį lygmenį jis turėjo sugerti (absorbuoti) fotoną, o į žemesnį emituoti (išspinduliuoti). Šis modelis buvo beveik tobulas, tik iškėlė vieną sudėtingą dilemą. Kaip gali elektronas nekirsdamas \“tarplygmeninės\“ zonos pereiti iš vieno lygmens į kitą.
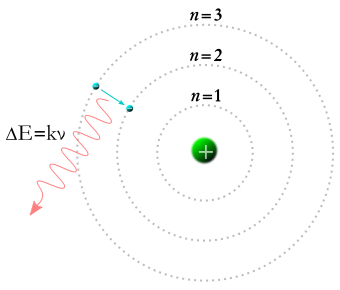
Čia pasineriame į stebuklingą kvantinės mechanikos pasaulį. Kitas (De Broilio) atomo modelis, paaiškinantis Boro modelį, buvo netikėtas ir sukėlė sąmišį. Jis teigė, kad elektronas nėra kamuoliukas skraidantis aplink branduolį, o banga. Tai reiškia, kad elektronas yra visose vieno lygmens dalyse vienu metu. Ir sugerdama fotoną tiesiog \“pastiprėja\“. Svarbu pastebėti, kad paveiksle rodomas kamuoliukas su e- simboliu tik parodo, kad vaizduojama banga yra elektronas. Jis jokiu būdu nerodo jo vietos tam tikru momentu.
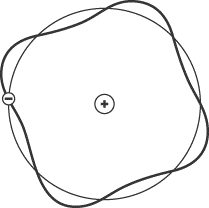
Net Enšteinui buvo sunku tuo patikėti. Tačiau netikėtumai tuo nesibaigė. Vienas garsiausių XXa. mokslininkų, kvantinės fizikos tėvas, Šriodingeris pristatė dar keistesnį modelį. Jo modelyje elektronas buvo galimybinė banga ir sugerdamas fotoną keisdavo galimybių išsidėstymą. Tai suprasti yra ypač sudėtinga (vienas mokslininkas net yra pasakęs \“Jei manai, kad supratai kvantinę mechaniką vadinasi apie ją tu dar negalvojai\“). Tarkime yra 80% tikimybė, kad elektronas bus pirmame lygmenyje, 10% tikimybė, kad antrame, 5.999999%, kad trečiame ir 0.00000001% tikimybės, kad elektronas skries link andromedos galaktikos. Absorbavęs fotoną jis turės 60% tikimybę būti antrame lygmenyje, 30% trečiame ir 10% ketvirtame (vadinasi jo galimybinė banga tiesiog pakeis padėtį). SVARBIAUSIA suprasti, kad ši tikimybė nereiškia jog elektronas bus arba taške A ar B ar C, o kad jis vienu metu yra visur tik atlikus eksperimentą 80 kartų iš šimto jį rasime taške A ir 1 kartą iš milijardo pakeliui į andromedą.

Apie tai kitame straipsnyje plačiai ir nuosekliai, tačiau manau, kad jau pajautėte kvantinės mechanikos skonį :).
Straipsnio autorius: Xpoint.

Naujausi komentarai